Лептинорезистентность и жировая болезнь печени, часть 4.
Все начинается с печени: лептинорезистентность и жировая болезнь, часть 4. Практически у каждого третьего человека (по другим данным – у каждого второго!) обнаруживаются изменения печени (жировая болезнь печени). Сегодня мы узнаем, что устойчивость к лептину начинается с изменений в печени. А так же узнаем, как опасен жир в печени, как его измерить и о чем он говорит.


Когда люди съедают еду, около 60% калорий оседает в печени, чтобы обеспечивать ткани энергией в промежутках между приёмами пищи. Другой гормон, глюкагон, опосредует освобождение этого топлива. Остальная энергия (40%) направляется к периферическим тканям и мышцам, где инсулин позволяет энергии проникать в клетки. Если эти клетки чувствительны к лептину, они проглотят все эти 40% калорий без остатка. Если же они устойчивы к лептину, лишние калории уйдут непосредственно обратно в печень, чтобы быть помещёнными в хранилище жира в жировых клетках (либо застрять внутри клеток печени), т.к. уровень инсулина высок. Чем больше жира уходит на хранение, тем выше уровни лептина становятся со временем. Если жир застревает в печени, это вызывает большие иммунные реакции, ведущие к множеству воспалительных химических веществ.
Таки образом, при ожирении, особенно висцеральном, увеличивается поступление в печень свободных жирных кислот, при этом развивается стеатоз печени (первый удар). В условиях инсулинорезистентности увеличивается липолиз в жировой ткани, а избыток СЖК поступает в печень. В итоге количество жирных кислот в гепатоците резко возрастает, формируется жировая дистрофия гепатоцитов. В литературе описано четыре механизма накопления жира в печени: увеличение поступления жира и свободных жирных кислот (СЖК) с пищей и захват их печенью из кровотока; усиление синтеза или угнетение процессов b-окисления СЖК в митохондриях гепатоцитов, что способствует усилению выработки триглицеридов (ТГ); нарушение выведения ТГ из гепатоцитов; углеводы, поступающие в печень из кровотока в избыточном количестве, также могут преобразовываться в жирные кислоты.
Увеличение притока СЖК и снижение скорости их окисления приводит к эстерификации СЖК с избыточным образованием триглицеридов в гепатоцитах и секреции повышенного количества липопротеидов очень низкой плотности (ЛПОНП), способствующих усилению свободнорадикального окисления липидов и накоплению продуктов их перекисного окисления («второй толчок»). В условиях повышенного поступления СЖК в печень возрастает роль микросомального окисления жирных кислот с участием цитохрома Р450 (CYP2E1 и CYP4A) и уменьшается Β-окисление СЖК в митохондриях, что приводит к образованию и накоплению реактивных форм кислорода, обладающих прямым цитотоксическим воздействием на гепатоциты и инициирующих процессы перекисного окисления липидов. На фоне нарастающей секреции провоспалительных цитокинов жировой тканью, в первую очередь ФНО-а, реактивные формы кислорода способствуют разобщению процесса окислительного фосфорилирования, истощению митохондриальной АТФ и, в конечном итоге, повреждению гепатоцитов и их некрозу
Одновременно или последовательно развивается окислительный стресс — «второй удар» с формированием воспалительной реакции и развитием стеатогепатита. Это связано в значительной степени с тем, что функциональная способность митохондрий истощается, включается микросомальное окисление липидов в системе цитохрома, что приводит к образованию активных форм кислорода и повышению продукции провоспалительных цитокининов с формированием воспаления в печени, гибели гепатоцитов, обусловленной цитотоксическими эффектами TNF-альфа1 — одного из основных индукторов апоптоза. ИЛ-6, -8 - провоспалительные цитокины, продуцируемые жировой тканью, являются «гепатоцитактивирующими факторами» и могут индуцировать синтез провоспалительных белков, таких как фибриноген и С-реактивный белок.
Таким образом, когда накопление жира в печени дошло до критического уровня, жир становится «плохим» начинает делать плохие вещи, выделяя воспалительные вещества (IL-6 и TNF альфа). Когда вы устойчивы к лептину, конечным результатом будет упаковка калорий в жир в той или иной форме ЛПНП. Эти порции ЛПНП покидают печень, потому что имеется физический лимит того, сколько жира может в ней находиться. Если этот процесс создания ЛПНП является хроническим и подавляет печень, жир накапливается внутри клеток печени и вызывает образование существенного количества реактивных форм кислорода (RoS). Это воспалительные химические вещества, которые коварно убивают клетки и лежат в основе всех хронических заболеваний, которые вы знаете.
Список заболеваний и ситуаций, при котором возникают «вторичные» НАЖБП и НАСГ, весьма широк и включает: синдром нарушенного всасывания, особенно при операциях по поводу ожирения, интенсивное снижение массы тела, длительное, несбалансированное парентеральное питание, болезни накопления.
Давайте разберемся, какую роль играет лептин в работе печени. Взаимосвязь лептина с НАЖБП была подтверждена последующим исследованием, которое показало, что как у мужчин, так и у женщин наблюдается гиперлептинемия. Но в то же время уровень лептина прямо коррелировал лишь со степенью стеатоза печени, но не являлся независимым предиктором ни воспалительного процесса, ни выраженности фиброза.
Лептин повышает чувствительность клеток печени и мышечной ткани к действию инсулина. Избыток лептина ведёт к подавлению секреции инсулина, ингибирует действие инсулина на клетки печени. Установлено, что в печени лептин обладает способностью тормозить глюконеогенез, путем влияния на активность фосфоэнолпируваткарбоксикиназы - фермента, ограничивающего скорость глюконеогенеза. Окисление жирных кислот лептин усиливает через стимуляцию AMP-активируемой протеинкиназы (AMPK). Гормон, ограничивая накопление триглицеридов в гепатоцитах, предотвращает «липотоксичность», и регулирует степень фиброза при репарации. Уровень лептина коррелирует с тяжестью стеатоза печени, но не зависит от активности воспаления или степени фиброза. Развитие стеатоза печени может быть связано с лептинорезистентностью.
Согласно многочисленным исследованиям, посвященным изучению клеточных и молекулярных механизмов, лежащих в основе профиброгенных эффектов лептина, этот адипокин оказывает биологическое воздействие на различные группы клеток, таких как клетки Купфера, синусоидальные эндотелиоциты и миофибробластоподобные клетки. Он усиливает фагоцитарную активность и выработку цитокинов купферовскими клетками и макрофагами, стимулирует пролиферацию эндотелиоцитов и продукцию ими активных форм кислорода . Кроме того, лептин оказывает прямое воздействие на стеллатные клетки печени (HSC), которые экспрессируют функционально активные лептиновые рецепторы. Выработка ObRb значительно увеличивается при трансдифференциации покоящейся HSC в миофибробластоподобную . Под воздействием лептина HSC вырабатывают повышенное количество проколлагена I типа и потенцируют эффекты трансформирующего фактора роста бета-1 (TGF-b1). Более того, под действием лептина происходит уменьшение распада фибротического экстрацеллюлярного коллагенового матрикса (ЭКМ), что характерно для фиброгенного процесса .
Лептин играет важную роль в процессе фиброгенеза в печени. Некоторыми исследованиями показано профиброгенное действие этого адипокина на печень. Дефицит лептина либо лептиновых рецепторов у лабораторных животных сопровождался значительным уменьшением фиброза в условиях экспериментального неалкогольного стеатогепатита (НАСГ), интоксикации тиоацетамидом, длительного воздействия четыреххлористого углерода и других моделей поражения печени. С другой стороны, введение лептина животным с острым либо хроническим повреждением печени сопровождалось существенным усилением выработки проколлагена I типа и профиброгенного цитокина трансформирующего фактора роста 1 (TGF-1).
Была установлена роль лептина в процессе ангиогенеза в печени. Активация лептиновых рецепторов в звездчатых клетках приводит к усиленной выработке сосудистого эндотелиального фактора роста (VEGF), мощного стимулятора образования новых сосудов в ткани. Неоваскуляризация печеночной ткани является еще одним механизмом профиброгенного действия лептина и существенно влияет на прогрессирование поражения печени при различных хронических заболеваниях. С другой стороны, доказанная взаимосвязь между ангиогенезом и онкогенезом позволяет предположить возможное участие лептина в развитии рака печени.
Так, на стадии стеатоза печени основным симптомом является гепатомегалия (обнаруженная случайно или при диспансерном обследовании). При повышении уровня трансаминаз необходимо проведение вирусологических исследований (которые либо подтвердят, либо отвергнут вирусные формы гепатита), а также диагностика других форм гепатита: аутоиммунного, билиарного, первичного склерозирующего холангита.
Диагноз чаще всего ставится при УЗИ печени, во многих случаях пациенты ранее даже не подозревали о наличии у них жировой дистрофии печени. При ультразвуковой диагностике наблюдается равномерное увеличение печени, диффузное повышение её эхогенности (иногда выраженное), с сохранением её однородности (хотя при прогрессировании процесса появляется характерная «зернистость» паренхимы, свидетельствующая о начале развития стеатогепатита и гепатита). УЗИ показывает изменения эхогенности, ультразвуковой проницаемости, структуры паренхимы и др., что может привести к заключению о наличии у пациента «диффузных изменений печени».
Термин «диффузные изменения печени» подразумевает множество заболеваний. По этой причине разнообразные диффузные поражения печени с точки зрения ультразвуковой диагностики целесообразно разделить на слабовыраженные и выраженные. Картина УЗИ может несколько различаться в зависимости от стадии и степени тяжести процесса, вида жировой инфильтрации, а также при комбинации этого заболевания с другими сопутствующими изменениями печени.
При компьютерной томографии выявляется в разной степени выраженное диффузное снижение денситометрических показателей паренхимы печени (ниже 55 HU, иногда вплоть до отрицательных значений, соответствующих плотности жира), как правило отмечается увеличение размеров органа. Возможно выявление ограниченных участков жировой инфильтрации, окружённых неизменённой тканью печени. Чаще локальная жировая инфильтрация наблюдается в S4 печени, имеет довольно ровные, прямые контуры, ход сосудов в инфильтрированной жиром ткани не изменён, масс-эффект (объёмное воздействие на окружающие структуры) отсутствует.
В настоящее время «золотым стандартом» диагностики НАЖБП считается пункционная биопсия печени, позволяющая объективно диагностировать НАЖБП, оценить степень активности НАСГ, стадию фиброза, прогнозировать течение заболевания, контролировать эффективность лечения. По данным исследований, практическая значимость диагностики НАЖБП до проведения биопсии с использованием неинвазивных методов составляет всего 50%. С 2005 года в клинической практике для комплексной оценки морфологических изменений в печени при НАЖБП широко используется шкала NAS (NAFLD activity score), предложенная D. A. Kleiner
Маркером НАЖБП может являться содержание в сыворотке крови фрагментов белка-филамента цитокератина-18 (CK18-Asp396), образующихся при его расщеплении активированными каспазами из гепатоцитов при апоптозе. Повышение уровней фрагментов цитокератина-18 является специфичным для стеатогепатита и позволяет дифференцировать его от стеатоза. Специфичность и чувствительность данного метода составляют 99,9% и 85,7% соответственно.

1. Вы жирные, если у вас жирная печень, вне зависимости от вашей массы тела.
2. Причин, ведущих к жировому повреждению печени, много: от переедания до токсического поражения алкоголем. Особой разницы в течении болезни нет.
3. Жирная печень провоцирует развитие системного воспаления, которое является причиной развития множества болезнией: от ожирения до сердечно-сосудистых и раковых заболеваний.
4. Состояние печени можно достаточно легко контролировать и отслеживать по ней свой прогресс.
5. Жирная печень чаще всего абсолютно бессимптомна и даже не проявляется на обычных анализах. Она, как и гипертензия, - молчаливый убийца.
Для понимания связи стресса, нашей реакции на него, важно знать, что
стресс практически всегда связан с накоплением «плохого» жира
(внутренний жир, висцеральный или абдоминальный жир). «Плохой жир»
вызывает воспаление, которое усиливает стресс и все движется по кругу.
Это режим дефицита, который проявляется во всех областях жизни человека:
в настроении, мотивации, энергичности, внешности, активности, весе,
болезнях, психике и даже в отношениях с другими
людьми. Как говорит народная мудрость, " с жиру бесятся".Но «плохой
жир» далеко не всегда связан с лишним весом. Кроме того, есть ведь и
"хороший" жир, который является отличным источником энергии.
Поэтому я разберу ряд случаев в неочевидным "плохим" жиром. Это жировая болезнь печени, это худые люди с внутренним ожирением и люди с нормальным весом, которые «жирные внутри». Для баланса, напишу про толстых людей, которые здоровы и не жирные. К сожалению, эти ньюансы мало кто учитывает, но они критически важны для здоровья. Вы худой и считаете себя не жирным? Тогда мы идем к вам! A точнее, к вашей печени!
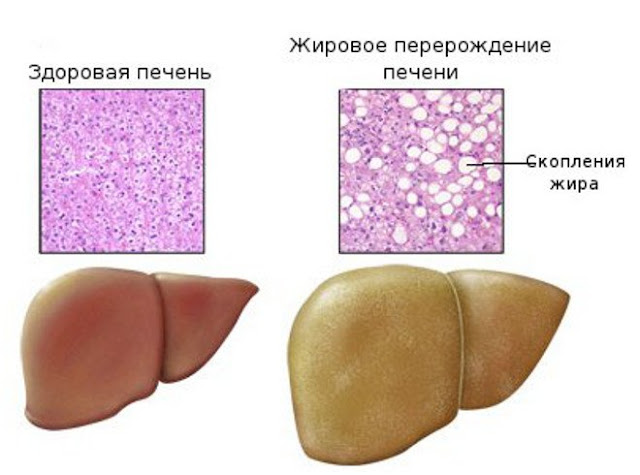
Жирная печень (жировая болезнь печени) – это тот рубикон, за которым переедание и выпивка превращается в реальную болезнь. Накопление жира в печени называют неалкогольной жировой болезнью печени (НАЖБП). Сразу скажу, что есть и алкогольная жировая болезнь печени, которая мало чем отличается (кроме причины). У НАЖБП существуют следующие варианты течения: стеатоз (тип 1) — преобладание жировой дистрофии гепатоцитов над всеми другими морфологическими изменениями, стеатогепатит (тип 2) — выраженные воспалительные инфильтраты как в строме, так и в паренхиме с наличием очаговых некрозов, стеатофиброз (тип 3) — преобладание фиброза портальной стромы, но без нарушения дольковой структуры, стеатоцирроз — нарушение дольковой структуры печени с наличием узлов-регенератов. НАЖБП может быть как проявлением различных заболеваний, так и самостоятельной патологией
Неалкогольный стеатоз печени (неалкогольная жировая болезнь печени (НАЖБП), жировая дистрофия печени, жировая печень, жировая инфильтрация) — первичное заболевание печени или синдром, формируемый избыточным накоплением жиров (преимущественно триглицеридов) в печени. В норме в печени содержится около 5% жира. Если рассматривать эту нозологию с количественной точки зрения, то «жир» должен составлять не менее 5–10% веса печени, или более 5% гепатоцитов должны содержать липиды (гистологически). Это немного! Т.е. болезнь уже активно протекает, если жир накопило более 5% клеток печени! Обратите внимание на этот факт!
1. Может протекать безсимптомно, обнаруживается случайно. У многих пациентов нарушения функции печени выявляют случайно во время обследования по поводу других заболеваний.
2. Имеет слабовыраженные симптомы. Течение заболевания, как правило, длительно, с минимальной или умеренно выраженной активностью воспаления в печени. У большинства пациентов симптомы, характерные для заболеваний печени, отсутствуют. Иногда имеются жалобы на тяжесть и неприятные ощущения в правом верхнем квадранте живота, усиливающиеся при движении, утомляемость, слабость, тошноту. Нередко заболевание диагностируется случайно, при ультразвуковом исследовании печени, когда обнаруживается ее увеличение и гиперэхогенность или «яркость» ткани печени вследствие диффузной жировой инфильтрации.
3. Если у вас нормальные анализы, то это не исключает проблем с печенью!! Повышенный уровень сывороточных трансаминаз выявляется лишь у 20–21% пациентов с НАЖБП. Тем не менее, нормальные показатели трансаминаз не исключают вероятность существования некротически-воспалительных изменений и фиброза печени.
3. Бывает у людей с нормальной массой тела. Увеличение ее распространенности параллельно эпидемии ожирения позволило для подтверждения жировой болезни печени использовать индекс массы тела (ИМТ). В то же время до 25 % больных с НАЖБП могут не страдать ожирением, но иметь четкие лабораторные доказательства ИР.
4. Очень медленно прогрессирует. Обычно стеатоз характеризуется стабильным, не прогрессирующим течением. Если же к жировой инфильтрации присоединяется воспалительный процесс, то есть развивается стеатогепатит, то заболевание часто прогрессирует с образованием фиброза печени (у 30-40 % больных) и цирроза (приблизительно у 10 %).
5. Жировая болезнь печени полностью обратима! Об этому будет позже. Необходимо отметить возможность обратного развития неалкогольной жировой болезни на фоне снижения веса (и-или висцерального жира).
6. Жировая болезнь печени очень распространена. Распространенность неалкогольного стеатоза печени у жителей экономически развитых стран мира составляет в среднем 2035%, неалкогольного стеатогепатита –3% [21, 29]. В США cтеатоз печени имеют 34% взрослого населения, в Японии – 29% [10, 36]. В России, по данным скрининговой программы по выявлению распространенности НАЖБП и ее клинических форм, проведенной в 2007 г. и охватившей 30754 человек, НАЖБП выявлена у 27% обследованных.
7. При ожирении проблема с печенью есть практически всегда. У больных ожирением распространенность различных клинических форм НАЖБП значительно выше, чем в общей популяции, и составляет, по данным исследований, до 93%. По данным G.Tarantino и соавт. (2007 г.), стеатоз выявляется у 10–25% населения США, из них в 57–75% – у лиц с морбидным (индекс массы тела >30–35) ожирением и почти в 100% – с ожирением и диабетом типа 2. При этом отмечается обратная связь: у больных НАЖБП ожирение выявляется в 30–100% случаев, диабет типа 2 – в 10–75%, гиперлипидемия – в 20–92% случаев.

Для развития жировой болезни нужно два удара. Первый удар - это плохое питание. При нем жир накапливается в печени. Второй удар – это воспаление и окисление (окислительный стресс). Жир окисляется и становится «плохим» жиром, т.е. выделяет вещества, провоцирующие воспаление. Помните, что в предыдущей статье я писал, что устойчивость лептина – это сочетание повышенного лептина и С-реактивного белка. Вот они и есть маркеры жировой болени, печени в том числе.
Удар по печени можно нанести не только фастфудом, но и алкоголем. Алкогольная жировая болезнь печени похожа не неалкогольную, а результат один и тот же! Прослежена прямая зависимость характера поражения печени от дозы ежедневно употребляемого алкоголя. Следует отметить, что тип напитка значения не имеет, важным является количество спирта. Было отмечено, что алкоголь является главной причиной печеночной патологии в Европе. Возможно сочетание алкогольной болезни печени и НАЖБП. Жировая дистрофия печени наиболее часто развивается у лиц с ожирением, злоупотребляющих алкоголем. Безопасные дозы алкоголя, которые не провоцируют прогрессирование НАЖБП, не установлены.
Поэтому я разберу ряд случаев в неочевидным "плохим" жиром. Это жировая болезнь печени, это худые люди с внутренним ожирением и люди с нормальным весом, которые «жирные внутри». Для баланса, напишу про толстых людей, которые здоровы и не жирные. К сожалению, эти ньюансы мало кто учитывает, но они критически важны для здоровья. Вы худой и считаете себя не жирным? Тогда мы идем к вам! A точнее, к вашей печени!
Жирная печень (жировая болезнь печени) – это тот рубикон, за которым переедание и выпивка превращается в реальную болезнь. Накопление жира в печени называют неалкогольной жировой болезнью печени (НАЖБП). Сразу скажу, что есть и алкогольная жировая болезнь печени, которая мало чем отличается (кроме причины). У НАЖБП существуют следующие варианты течения: стеатоз (тип 1) — преобладание жировой дистрофии гепатоцитов над всеми другими морфологическими изменениями, стеатогепатит (тип 2) — выраженные воспалительные инфильтраты как в строме, так и в паренхиме с наличием очаговых некрозов, стеатофиброз (тип 3) — преобладание фиброза портальной стромы, но без нарушения дольковой структуры, стеатоцирроз — нарушение дольковой структуры печени с наличием узлов-регенератов. НАЖБП может быть как проявлением различных заболеваний, так и самостоятельной патологией
Неалкогольный стеатоз печени (неалкогольная жировая болезнь печени (НАЖБП), жировая дистрофия печени, жировая печень, жировая инфильтрация) — первичное заболевание печени или синдром, формируемый избыточным накоплением жиров (преимущественно триглицеридов) в печени. В норме в печени содержится около 5% жира. Если рассматривать эту нозологию с количественной точки зрения, то «жир» должен составлять не менее 5–10% веса печени, или более 5% гепатоцитов должны содержать липиды (гистологически). Это немного! Т.е. болезнь уже активно протекает, если жир накопило более 5% клеток печени! Обратите внимание на этот факт!
 |
| лептинорезистентность и жировая болезнь печени |
Особенности течения и проявления жировой болезни печени.
1. Может протекать безсимптомно, обнаруживается случайно. У многих пациентов нарушения функции печени выявляют случайно во время обследования по поводу других заболеваний.
2. Имеет слабовыраженные симптомы. Течение заболевания, как правило, длительно, с минимальной или умеренно выраженной активностью воспаления в печени. У большинства пациентов симптомы, характерные для заболеваний печени, отсутствуют. Иногда имеются жалобы на тяжесть и неприятные ощущения в правом верхнем квадранте живота, усиливающиеся при движении, утомляемость, слабость, тошноту. Нередко заболевание диагностируется случайно, при ультразвуковом исследовании печени, когда обнаруживается ее увеличение и гиперэхогенность или «яркость» ткани печени вследствие диффузной жировой инфильтрации.
3. Если у вас нормальные анализы, то это не исключает проблем с печенью!! Повышенный уровень сывороточных трансаминаз выявляется лишь у 20–21% пациентов с НАЖБП. Тем не менее, нормальные показатели трансаминаз не исключают вероятность существования некротически-воспалительных изменений и фиброза печени.
3. Бывает у людей с нормальной массой тела. Увеличение ее распространенности параллельно эпидемии ожирения позволило для подтверждения жировой болезни печени использовать индекс массы тела (ИМТ). В то же время до 25 % больных с НАЖБП могут не страдать ожирением, но иметь четкие лабораторные доказательства ИР.
4. Очень медленно прогрессирует. Обычно стеатоз характеризуется стабильным, не прогрессирующим течением. Если же к жировой инфильтрации присоединяется воспалительный процесс, то есть развивается стеатогепатит, то заболевание часто прогрессирует с образованием фиброза печени (у 30-40 % больных) и цирроза (приблизительно у 10 %).
5. Жировая болезнь печени полностью обратима! Об этому будет позже. Необходимо отметить возможность обратного развития неалкогольной жировой болезни на фоне снижения веса (и-или висцерального жира).
6. Жировая болезнь печени очень распространена. Распространенность неалкогольного стеатоза печени у жителей экономически развитых стран мира составляет в среднем 2035%, неалкогольного стеатогепатита –3% [21, 29]. В США cтеатоз печени имеют 34% взрослого населения, в Японии – 29% [10, 36]. В России, по данным скрининговой программы по выявлению распространенности НАЖБП и ее клинических форм, проведенной в 2007 г. и охватившей 30754 человек, НАЖБП выявлена у 27% обследованных.
7. При ожирении проблема с печенью есть практически всегда. У больных ожирением распространенность различных клинических форм НАЖБП значительно выше, чем в общей популяции, и составляет, по данным исследований, до 93%. По данным G.Tarantino и соавт. (2007 г.), стеатоз выявляется у 10–25% населения США, из них в 57–75% – у лиц с морбидным (индекс массы тела >30–35) ожирением и почти в 100% – с ожирением и диабетом типа 2. При этом отмечается обратная связь: у больных НАЖБП ожирение выявляется в 30–100% случаев, диабет типа 2 – в 10–75%, гиперлипидемия – в 20–92% случаев.

Как развивается жировая болезнь печени?
Для развития жировой болезни нужно два удара. Первый удар - это плохое питание. При нем жир накапливается в печени. Второй удар – это воспаление и окисление (окислительный стресс). Жир окисляется и становится «плохим» жиром, т.е. выделяет вещества, провоцирующие воспаление. Помните, что в предыдущей статье я писал, что устойчивость лептина – это сочетание повышенного лептина и С-реактивного белка. Вот они и есть маркеры жировой болени, печени в том числе.
Удар по печени можно нанести не только фастфудом, но и алкоголем. Алкогольная жировая болезнь печени похожа не неалкогольную, а результат один и тот же! Прослежена прямая зависимость характера поражения печени от дозы ежедневно употребляемого алкоголя. Следует отметить, что тип напитка значения не имеет, важным является количество спирта. Было отмечено, что алкоголь является главной причиной печеночной патологии в Европе. Возможно сочетание алкогольной болезни печени и НАЖБП. Жировая дистрофия печени наиболее часто развивается у лиц с ожирением, злоупотребляющих алкоголем. Безопасные дозы алкоголя, которые не провоцируют прогрессирование НАЖБП, не установлены.


Первый удар (жир накапливается)
Когда люди съедают еду, около 60% калорий оседает в печени, чтобы обеспечивать ткани энергией в промежутках между приёмами пищи. Другой гормон, глюкагон, опосредует освобождение этого топлива. Остальная энергия (40%) направляется к периферическим тканям и мышцам, где инсулин позволяет энергии проникать в клетки. Если эти клетки чувствительны к лептину, они проглотят все эти 40% калорий без остатка. Если же они устойчивы к лептину, лишние калории уйдут непосредственно обратно в печень, чтобы быть помещёнными в хранилище жира в жировых клетках (либо застрять внутри клеток печени), т.к. уровень инсулина высок. Чем больше жира уходит на хранение, тем выше уровни лептина становятся со временем. Если жир застревает в печени, это вызывает большие иммунные реакции, ведущие к множеству воспалительных химических веществ.
Таки образом, при ожирении, особенно висцеральном, увеличивается поступление в печень свободных жирных кислот, при этом развивается стеатоз печени (первый удар). В условиях инсулинорезистентности увеличивается липолиз в жировой ткани, а избыток СЖК поступает в печень. В итоге количество жирных кислот в гепатоците резко возрастает, формируется жировая дистрофия гепатоцитов. В литературе описано четыре механизма накопления жира в печени: увеличение поступления жира и свободных жирных кислот (СЖК) с пищей и захват их печенью из кровотока; усиление синтеза или угнетение процессов b-окисления СЖК в митохондриях гепатоцитов, что способствует усилению выработки триглицеридов (ТГ); нарушение выведения ТГ из гепатоцитов; углеводы, поступающие в печень из кровотока в избыточном количестве, также могут преобразовываться в жирные кислоты.
Увеличение притока СЖК и снижение скорости их окисления приводит к эстерификации СЖК с избыточным образованием триглицеридов в гепатоцитах и секреции повышенного количества липопротеидов очень низкой плотности (ЛПОНП), способствующих усилению свободнорадикального окисления липидов и накоплению продуктов их перекисного окисления («второй толчок»). В условиях повышенного поступления СЖК в печень возрастает роль микросомального окисления жирных кислот с участием цитохрома Р450 (CYP2E1 и CYP4A) и уменьшается Β-окисление СЖК в митохондриях, что приводит к образованию и накоплению реактивных форм кислорода, обладающих прямым цитотоксическим воздействием на гепатоциты и инициирующих процессы перекисного окисления липидов. На фоне нарастающей секреции провоспалительных цитокинов жировой тканью, в первую очередь ФНО-а, реактивные формы кислорода способствуют разобщению процесса окислительного фосфорилирования, истощению митохондриальной АТФ и, в конечном итоге, повреждению гепатоцитов и их некрозу
Второй удар (жир воспаляется и окисляется)
Одновременно или последовательно развивается окислительный стресс — «второй удар» с формированием воспалительной реакции и развитием стеатогепатита. Это связано в значительной степени с тем, что функциональная способность митохондрий истощается, включается микросомальное окисление липидов в системе цитохрома, что приводит к образованию активных форм кислорода и повышению продукции провоспалительных цитокининов с формированием воспаления в печени, гибели гепатоцитов, обусловленной цитотоксическими эффектами TNF-альфа1 — одного из основных индукторов апоптоза. ИЛ-6, -8 - провоспалительные цитокины, продуцируемые жировой тканью, являются «гепатоцитактивирующими факторами» и могут индуцировать синтез провоспалительных белков, таких как фибриноген и С-реактивный белок.
Таким образом, когда накопление жира в печени дошло до критического уровня, жир становится «плохим» начинает делать плохие вещи, выделяя воспалительные вещества (IL-6 и TNF альфа). Когда вы устойчивы к лептину, конечным результатом будет упаковка калорий в жир в той или иной форме ЛПНП. Эти порции ЛПНП покидают печень, потому что имеется физический лимит того, сколько жира может в ней находиться. Если этот процесс создания ЛПНП является хроническим и подавляет печень, жир накапливается внутри клеток печени и вызывает образование существенного количества реактивных форм кислорода (RoS). Это воспалительные химические вещества, которые коварно убивают клетки и лежат в основе всех хронических заболеваний, которые вы знаете.
Список заболеваний и ситуаций, при котором возникают «вторичные» НАЖБП и НАСГ, весьма широк и включает: синдром нарушенного всасывания, особенно при операциях по поводу ожирения, интенсивное снижение массы тела, длительное, несбалансированное парентеральное питание, болезни накопления.
Лептин и печень.
Давайте разберемся, какую роль играет лептин в работе печени. Взаимосвязь лептина с НАЖБП была подтверждена последующим исследованием, которое показало, что как у мужчин, так и у женщин наблюдается гиперлептинемия. Но в то же время уровень лептина прямо коррелировал лишь со степенью стеатоза печени, но не являлся независимым предиктором ни воспалительного процесса, ни выраженности фиброза.
Лептин повышает чувствительность клеток печени и мышечной ткани к действию инсулина. Избыток лептина ведёт к подавлению секреции инсулина, ингибирует действие инсулина на клетки печени. Установлено, что в печени лептин обладает способностью тормозить глюконеогенез, путем влияния на активность фосфоэнолпируваткарбоксикиназы - фермента, ограничивающего скорость глюконеогенеза. Окисление жирных кислот лептин усиливает через стимуляцию AMP-активируемой протеинкиназы (AMPK). Гормон, ограничивая накопление триглицеридов в гепатоцитах, предотвращает «липотоксичность», и регулирует степень фиброза при репарации. Уровень лептина коррелирует с тяжестью стеатоза печени, но не зависит от активности воспаления или степени фиброза. Развитие стеатоза печени может быть связано с лептинорезистентностью.
Согласно многочисленным исследованиям, посвященным изучению клеточных и молекулярных механизмов, лежащих в основе профиброгенных эффектов лептина, этот адипокин оказывает биологическое воздействие на различные группы клеток, таких как клетки Купфера, синусоидальные эндотелиоциты и миофибробластоподобные клетки. Он усиливает фагоцитарную активность и выработку цитокинов купферовскими клетками и макрофагами, стимулирует пролиферацию эндотелиоцитов и продукцию ими активных форм кислорода . Кроме того, лептин оказывает прямое воздействие на стеллатные клетки печени (HSC), которые экспрессируют функционально активные лептиновые рецепторы. Выработка ObRb значительно увеличивается при трансдифференциации покоящейся HSC в миофибробластоподобную . Под воздействием лептина HSC вырабатывают повышенное количество проколлагена I типа и потенцируют эффекты трансформирующего фактора роста бета-1 (TGF-b1). Более того, под действием лептина происходит уменьшение распада фибротического экстрацеллюлярного коллагенового матрикса (ЭКМ), что характерно для фиброгенного процесса .
Лептин играет важную роль в процессе фиброгенеза в печени. Некоторыми исследованиями показано профиброгенное действие этого адипокина на печень. Дефицит лептина либо лептиновых рецепторов у лабораторных животных сопровождался значительным уменьшением фиброза в условиях экспериментального неалкогольного стеатогепатита (НАСГ), интоксикации тиоацетамидом, длительного воздействия четыреххлористого углерода и других моделей поражения печени. С другой стороны, введение лептина животным с острым либо хроническим повреждением печени сопровождалось существенным усилением выработки проколлагена I типа и профиброгенного цитокина трансформирующего фактора роста 1 (TGF-1).
Была установлена роль лептина в процессе ангиогенеза в печени. Активация лептиновых рецепторов в звездчатых клетках приводит к усиленной выработке сосудистого эндотелиального фактора роста (VEGF), мощного стимулятора образования новых сосудов в ткани. Неоваскуляризация печеночной ткани является еще одним механизмом профиброгенного действия лептина и существенно влияет на прогрессирование поражения печени при различных хронических заболеваниях. С другой стороны, доказанная взаимосвязь между ангиогенезом и онкогенезом позволяет предположить возможное участие лептина в развитии рака печени.
 |
| лептинорезистентность и жировая болезнь печени |
Диагностика жировой болезни печени
Так, на стадии стеатоза печени основным симптомом является гепатомегалия (обнаруженная случайно или при диспансерном обследовании). При повышении уровня трансаминаз необходимо проведение вирусологических исследований (которые либо подтвердят, либо отвергнут вирусные формы гепатита), а также диагностика других форм гепатита: аутоиммунного, билиарного, первичного склерозирующего холангита.
Диагноз чаще всего ставится при УЗИ печени, во многих случаях пациенты ранее даже не подозревали о наличии у них жировой дистрофии печени. При ультразвуковой диагностике наблюдается равномерное увеличение печени, диффузное повышение её эхогенности (иногда выраженное), с сохранением её однородности (хотя при прогрессировании процесса появляется характерная «зернистость» паренхимы, свидетельствующая о начале развития стеатогепатита и гепатита). УЗИ показывает изменения эхогенности, ультразвуковой проницаемости, структуры паренхимы и др., что может привести к заключению о наличии у пациента «диффузных изменений печени».
Термин «диффузные изменения печени» подразумевает множество заболеваний. По этой причине разнообразные диффузные поражения печени с точки зрения ультразвуковой диагностики целесообразно разделить на слабовыраженные и выраженные. Картина УЗИ может несколько различаться в зависимости от стадии и степени тяжести процесса, вида жировой инфильтрации, а также при комбинации этого заболевания с другими сопутствующими изменениями печени.
При компьютерной томографии выявляется в разной степени выраженное диффузное снижение денситометрических показателей паренхимы печени (ниже 55 HU, иногда вплоть до отрицательных значений, соответствующих плотности жира), как правило отмечается увеличение размеров органа. Возможно выявление ограниченных участков жировой инфильтрации, окружённых неизменённой тканью печени. Чаще локальная жировая инфильтрация наблюдается в S4 печени, имеет довольно ровные, прямые контуры, ход сосудов в инфильтрированной жиром ткани не изменён, масс-эффект (объёмное воздействие на окружающие структуры) отсутствует.
В настоящее время «золотым стандартом» диагностики НАЖБП считается пункционная биопсия печени, позволяющая объективно диагностировать НАЖБП, оценить степень активности НАСГ, стадию фиброза, прогнозировать течение заболевания, контролировать эффективность лечения. По данным исследований, практическая значимость диагностики НАЖБП до проведения биопсии с использованием неинвазивных методов составляет всего 50%. С 2005 года в клинической практике для комплексной оценки морфологических изменений в печени при НАЖБП широко используется шкала NAS (NAFLD activity score), предложенная D. A. Kleiner
Маркером НАЖБП может являться содержание в сыворотке крови фрагментов белка-филамента цитокератина-18 (CK18-Asp396), образующихся при его расщеплении активированными каспазами из гепатоцитов при апоптозе. Повышение уровней фрагментов цитокератина-18 является специфичным для стеатогепатита и позволяет дифференцировать его от стеатоза. Специфичность и чувствительность данного метода составляют 99,9% и 85,7% соответственно.

Заключение.
1. Вы жирные, если у вас жирная печень, вне зависимости от вашей массы тела.
2. Причин, ведущих к жировому повреждению печени, много: от переедания до токсического поражения алкоголем. Особой разницы в течении болезни нет.
3. Жирная печень провоцирует развитие системного воспаления, которое является причиной развития множества болезнией: от ожирения до сердечно-сосудистых и раковых заболеваний.
4. Состояние печени можно достаточно легко контролировать и отслеживать по ней свой прогресс.
5. Жирная печень чаще всего абсолютно бессимптомна и даже не проявляется на обычных анализах. Она, как и гипертензия, - молчаливый убийца.
Комментарии